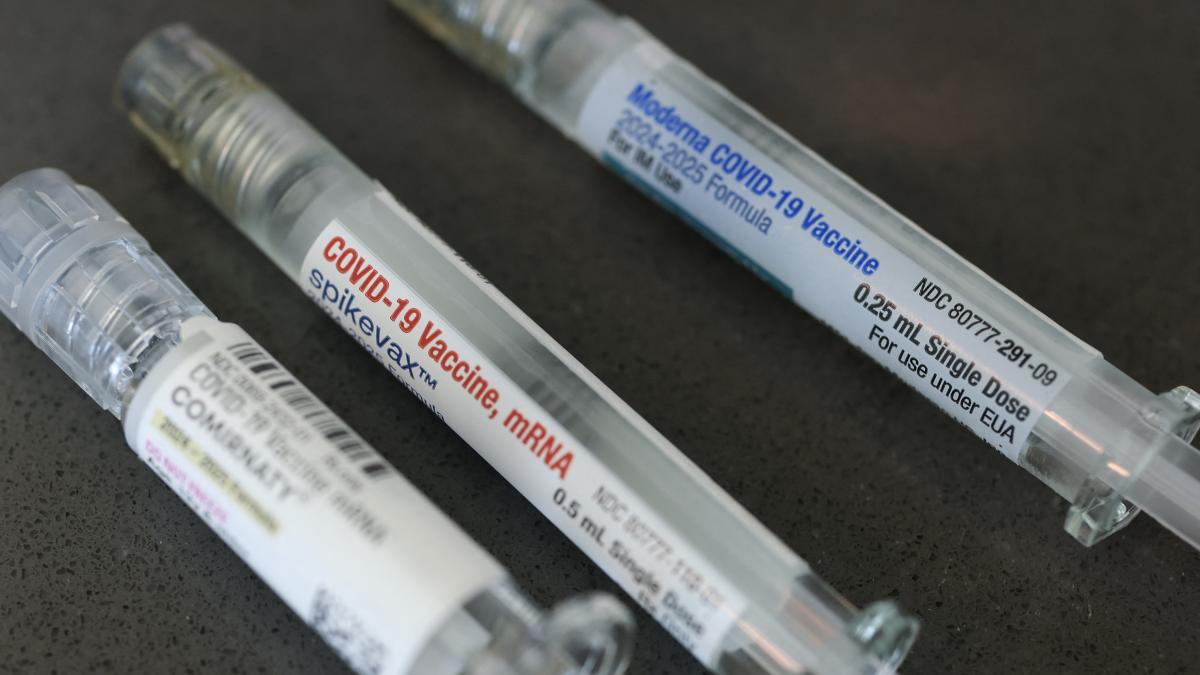
Los laboratorios Pfizer y BioNTech decidieron dar por finalizado un importante ensayo clínico en territorio estadounidense dedicado a evaluar su vacuna contra el Covid-19 de nueva generación en personas adultas sanas entre 50 y 64 años. La razón principal citada por ambas compañías fue la imposibilidad de alcanzar el número requerido de voluntarios para el estudio. Mediante una comunicación dirigida a los investigadores participantes el 30 de marzo, Pfizer informó que cessaría el monitoreo de síntomas de Covid-19 en todos los integrantes del ensayo a partir del 3 de abril. El período de inscripción se cerró el 6 de marzo tras evaluar las condiciones epidemiológicas vigentes. Esta decisión ocurre mientras las empresas productoras de vacunas contra el Covid-19 enfrentan presiones gubernamentales y una demanda limitada de sus productos en el mercado estadounidense. La Administración de Alimentos y Medicamentos estadounidense intensificó durante el año anterior sus normas para la aplicación de vacunas, requiriendo ensayos amplios con grupo placebo en personas de 50 a 64 años como requisito para incluir la vacuna en sus recomendaciones oficiales. Pfizer y BioNTech comunicaron a las autoridades regulatorias su intención de abandonar el estudio debido a las dificultades para reclutar participantes suficientes. El número objetivo establecido era entre 25.000 y 30.000 voluntarios aproximadamente. En un comunicado conjunto, las compañías expresaron que la interrupción del estudio no obedecía a inquietudes sobre seguridad o el balance riesgo-beneficio, sino a la lentitud en la captación de participantes que impedía obtener información relevante posterior al lanzamiento comercial. Las cotizaciones bursátiles de ambas empresas experimentaron movimientos positivos, con Pfizer y Moderna subiendo cercano al 1 por ciento, mientras que BioNTech mostró un incremento de alrededor del 2 por ciento. Vinay Prasad, encargado de vacunas en la FDA que había promovido la realización de ensayos controlados con placebo, se retirará de la agencia este mes. Analistas del sector advirtieron que imponer nuevos ensayos amplios podría resultar en retrasos o limitaciones en la disponibilidad de vacunas modernizadas para poblaciones de bajo riesgo. El camino regulatorio hacia la aprobación para este grupo etario permanece incierto. La FDA no realizó declaraciones inmediatas al respecto. Las compañías tampoco ofrecieron detalles sobre sus estrategias comerciales para esta franja de edad. Este cierre antecede a la reunión prevista en mayo del Comité Asesor de Vacunas de la FDA, que habría utilizado los datos generados para orientar decisiones futuras sobre la aplicación de vacunas actualizadas.
- contacto@lagacetamexico.com
- Lun - Dom: 8:00 - 20:00